肝胆膵領域の癌には難治性の癌腫が多く、疫学的にも増加傾向です。平成26年度の厚生統計要覧によれば、日本における年間死亡者数は肝臓癌約3万人、胆道癌約1万8千人、膵臓癌約3万人と報告されています。これらの癌腫の死亡率は発生率とほぼ同じであり、他の癌腫と比較して予後不良です。2016年1月に国立がん研究センターにより集計されたがんの部位別10年生存率は、肝臓癌15.3%、胆道癌19.7%、膵臓癌4.9%と、すべてのがんの全臨床病期の10年相対生存率58.2%と比べても極めて低い状況です。
このように予後不良な肝胆膵腫瘍に対しては、さらなる治療成績の向上を目指して治療成績の検証を行うとともに、安全で確実な治療法を実践するための検討を行うことが重要と考えられます。また癌の病態の理解を深め、新規の治療標的の同定や治療法の開発を目指すことが必要です。一方、肝胆膵領域には癌との鑑別を要する病変や手術を要する良性疾患が多く存在します。近年、そうした良性疾患に対しては腹腔鏡手術などの低侵襲手術が積極的に導入され、治療の選択肢が広がりつつあります。そうしたなかで、治療の安全性や根治性に対するエビデンスの確立が求められています。
肝胆膵領域の疾患に関わるこうした種々の課題に対し、当教室では基礎研究から臨床研究、臨床試験まで様々な分野の研究を行っております。
基礎的な研究のテーマとしては、癌関連線維芽細胞(CAF)やユビキチンリガーゼの一種でがん抑制因子と考えられているFBXW7、細胞房室-核輸送タンパクとしてがんの悪性度に関わるとされるKPNA2、細胞内シグナル伝達において重要とされるRAB5等に注目し、肝胆膵癌における新規バイオマーカーや治療戦略の開発を目指し、基礎研究に取り組んでいます。
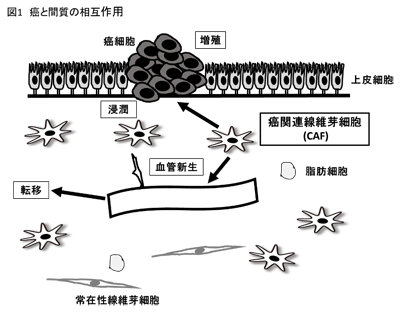
肝細胞癌の予後は不良で、近年は明らかなウイルス肝炎感染を伴わない肝癌が増加傾向です。手術、抗癌剤、放射線治療が行われていますが、治療効果は十分でなく、新たな治療戦略が求められています。癌組織は癌細胞と周囲の間質から構成されますが、近年、癌の微小環境において両者の相互作用が極めて重要と報告されています。中でも癌間質の主な構成要素である癌関連線維芽細胞(CAF)の機能が注目されています。我々はこれまでに、Conophyllineが肝星細胞の活性化および線維化を抑制することを報告してきました。本研究では、CAFの役割を明らかにするとともに、Conophyllineの線維化抑制によるCAFの制御の可能性を検討し、肝癌に対する新たな治療戦略を開発することを目的としています。
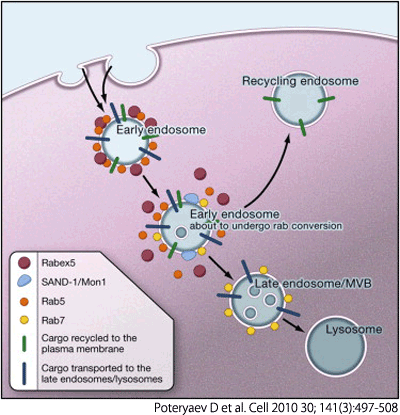
RAB蛋白は低分子量GTPaseの一種で、細胞膜蛋白の細胞内取り込みに関与し、細胞内シグナル伝達で重要な機能を有しています。RAB蛋白の一つであるRAB5は、上皮マーカーE-cadherinの細胞内取り込みを介し、癌の悪性度に関連する上皮間葉移行(EMT)の誘導因子として報告されています。これまでに複数の癌腫においてRAB5の過剰発現が報告されていますが、膵癌における発現意義は不明であり、当科における膵癌切除症例を対象として発現意義の検討を行っております。
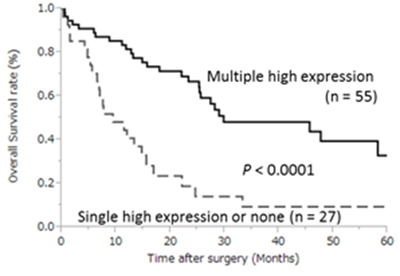
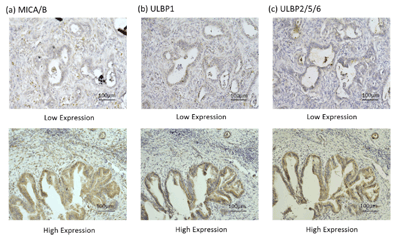
NKG2Dリガンドは癌細胞上に発現する免疫調節性のリガンドとして知られています。NK細胞やNKT細胞上に発現するNKG2Dレセプターを介して、腫瘍免疫応答を活性化するとされ、これまでいくつかの癌腫において高発現が報告されてしました。当科における胆管癌切除症例を対象として発現意義の検討を行ったところ、高発現群では低発現群と比較して有意に予後良好であることがわかりました。また複数のNKG2Dリガンド発現とNKG2Dレセプター発現の相互作用が腫瘍進行抑制に重要である可能性が示唆され、NKG2Dリガンド発現のメカニズムについて研究を進めております。
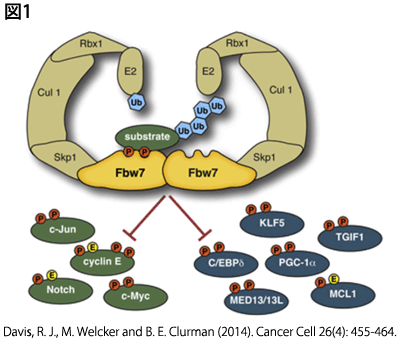
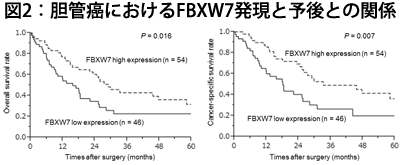
SCF(Skp1,Cullin-1, F box protein)ユビキチンリガーゼのF box proteinの一種であるFBXW7は細胞周期関連因子および腫瘍性タンパクのユビキチン化を担っており、細胞周期調節因子および腫瘍抑制因子と考えられています(図1)。FBXW7低発現では腫瘍性タンパクの蓄積を介し、癌の進展に関わることが報告されており、当科でも以前より胃癌、食道癌、肺非小細胞肺癌においてFBXW7の発現が腫瘍の悪性度や予後、抗癌剤の感受性に関与していることを報告してきました[1-3]。将来の治療標的としても有望視されており、当科では引き続き、難治性癌である胆管癌・膵癌を対象に切除検体を用いたFBXW7発現の臨床的意義(図2)、および細胞株のFBXW7発現の抑制および過剰発現モデルを用いて胆管癌・膵癌におけるFBXW7の機能解析を行っています。